多発性骨髄腫の治療
Q.多発性骨髄腫では、どのような治療が行われるのですか
A.症候性骨髄腫の治療には、大量薬物療法に自家造血幹細胞移植を併用する方法、あるいは新規薬剤を組み合わせた治療があります。症状を改善する治療も重要で、合併症の改善が骨髄腫の治療より優先されることもあります。
治療は、一般的に、高カルシウム血症、腎障害、貧血、骨病変といったCRAB症状が出た段階で開始します。
ただ、進行するリスクが高い骨髄腫診断バイオマーカー(図表8)の①に当てはまる場合には95%、②③なら70%の患者さんが2年以内に症候性骨髄腫に進行します。そのため、症状が出ていない段階から骨髄腫の治療を始める場合があります。

治療を行う場合には、まずは、2~4種類の薬を組み合わせた薬物療法を行い、体の中の骨髄腫細胞をできる限り減らす導入療法を行います。導入療法は、寛解を誘導する治療です。薬物療法の内容は、患者さんの年齢、体力、臓器障害の有無、リスクの高い染色体・遺伝子異常の有無(「多発性骨髄腫の検査」図表4)などによって異なります。
多発性骨髄腫では、最初の治療が非常に重要であり、一連の治療により微小残存病変(MRD:Minimal Residual Disease)が陰性になるくらい深い寛解を目指します(コラム「MRDがみられないぐらいの寛解を目指す」)。65歳以下(あるいは70歳未満)で感染症や肝障害、腎障害がなく、心臓や肺の機能にも問題がなく、本人が希望した場合には、大量薬物療法と自家造血幹細胞移植を組み合わせた治療を行います。年齢や臓器障害などにより移植の適応にならない場合には、新規薬剤(新しいタイプの薬)を組み合わせた治療を行います。
骨髄腫の治療は、日本血液学会の『造血器腫瘍診療ガイドライン』、日本骨髄腫学会の『多発性骨髄腫の診療指針』によって標準化されています。標準治療は、国内外のたくさんの臨床試験の結果をもとに科学的に検証され、専門家の間で合意が得られている現時点で最適な治療法です。
MRDがみられないぐらいの寛解を目指す
顕微鏡では検出できない分子学的なレベルの微小な残存病変がMRDです。
骨髄検査で採取した病変をマルチパラメーターフローサイトメトリーという解析方法で調べ、PET(陽電子放射断層撮影)-CTなどの画像検査の結果と合わせてMRDの有無を調べます。
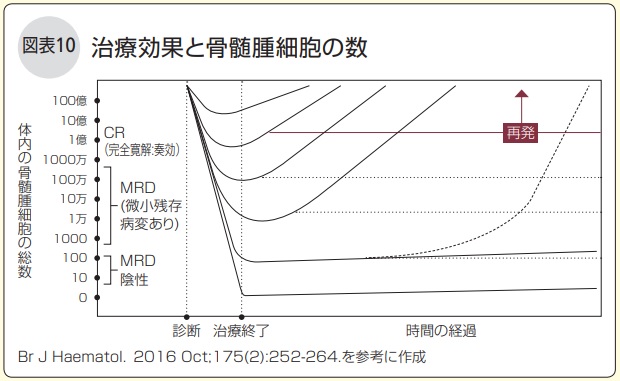
MRDが検出されないMRD陰性になると、再発せずに過ごせる期間が長く続く可能性が高まります。体内の骨髄腫細胞の数がゼロに近づくほど、再発せずに過ごせる期間が長くなります(図表10)。
つまり、治療の目的は、MRDがみられなくなるくらいの寛解を目指すことです。
完全寛解とは?
血液中、尿中のM蛋白がなくなって造血機能が回復し、多発性骨髄腫による症状もなくなった状態です。①血液中にも尿中にもM蛋白が検出されない、②軟部組織に腫瘤が確認できない、③骨髄中の形質細胞が5%未満、この3つのすべてを満たした場合に、完全寛解(奏効:CR)と判断されます。また、①~③に加え、遊離軽鎖の比が2回以上正常範囲、かつ、骨髄生検で採取した組織を免疫染色(κ、λ)しても骨髄中に異常形質細胞がないときには、厳密完全寛解の状態です。ただし、完全寛解になっても見えないところに骨髄腫細胞が残っている可能性があり、治癒ではないことは知っておきましょう。
臨床試験とは?
新薬や治療法を開発するために、ヒトを対象に有効性と安全性を科学的に調べるのが「臨床試験」です。臨床試験には第1相:安全性の確認、第2相:有効性・安全性の確認、第3相:標準治療との比較による有効性・安全性の総合評価の3段階があります。現在の標準治療も過去の臨床試験で有効性や安全性が認められたものです。多発性骨髄腫の分野でも、現在の標準治療より、さらに効果と安全性の高い治療法の確立を目指して複数の臨床試験が行われています。臨床試験に参加したいときは担当医に相談してみましょう。
●移植を受ける人の治療法
プロテアソーム阻害薬のボルテゾミブや免疫調節薬のレナリドミドなどの新規薬剤を用いた導入療法の後、患者さん自身の末梢血造血幹細胞を採取し、大量薬物療法と自家造血幹細胞移植を組み合わせた治療を行います(図表9)。
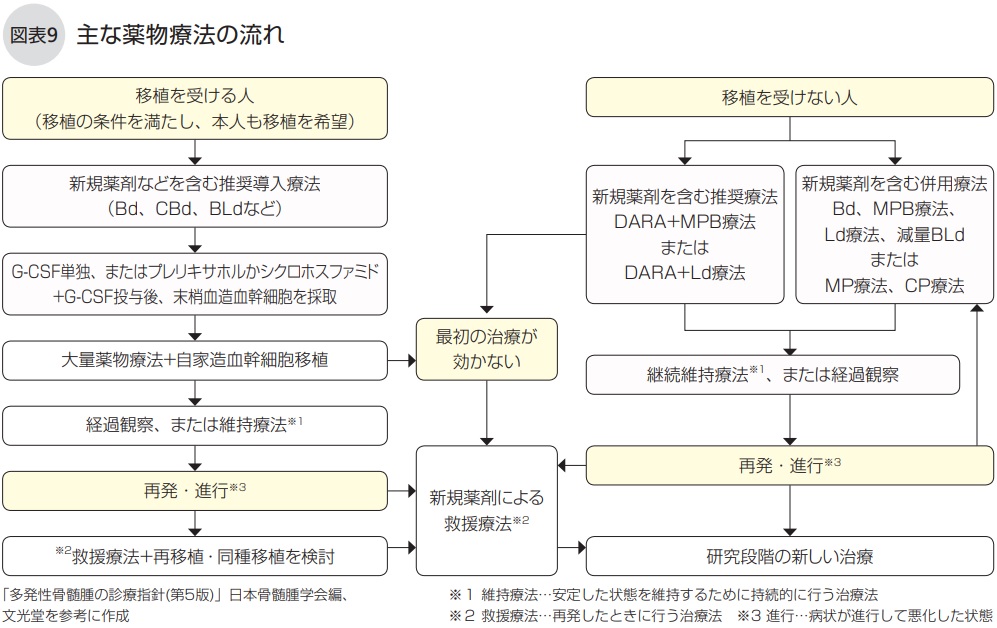
標準治療として推奨される導入療法には、①ボルテゾミブ+デキサメタゾン(Bd)、②シクロホスファミド+Bd(CBd)、③Bd+レナリドミド(BLd)などの2~3剤併用療法があります。
デキサメタゾン、レナリドミドは内服薬、それ以外は注射薬です。
ボルテゾミブは腎障害がある場合には有効です。ボルテゾミブによる間質性肺炎、末梢神経障害などの副作用を避けたい場合にはレナリドミドの併用療法などを検討します。3剤併用療法は、2剤併用療法よりも効果が高い半面、副作用も強くなる場合があるので注意が必要です。
移植を受ける人は、導入療法を3~4コース行った後、白血球を増やすG-CSF(顆粒球コロニー刺激因子)などを注射して自分の末梢血より造血幹細胞を採取し凍結保存します。
その後、点滴薬のメルファランを2日間大量投与し、自家造血幹細胞移植を行って造血機能を回復させます。腎障害が高度な場合などは、メルファランを減薬します。
骨髄腫細胞が骨髄に見つからない状態になり、血清遊離軽鎖(FLC)比が正常化するなど治療効果が十分得られたら、休薬して経過観察をするか、維持療法を行います。
維持療法は、再発を予防し、できるだけ長く寛解状態を維持するために行う治療です。自家造血幹細胞移植後の維持療法には、内服薬のイキサゾミブを2年間服用する方法があります。高リスクの染色体・遺伝子異常のある人も含めて再発予防効果が認められ、内服薬なので、投与のために通院しなくても済むのが利点です。
レナリドミドを用いた維持療法は、再発を遅らせる効果が報告されています。ただし、レナリドミドは二次発がんのリスクがあるため、維持療法を行うかどうか、行った場合はいつまで続けるか慎重な判断が必要です。
ボルテゾミブやレナリドミドなどの新規薬剤を用いた初回治療によってMRDが検出できないくらい深い治療効果が得られれば、症状のない状態で長期間生存する可能性がより高くなります。
●移植を受けない人の治療法
標準治療として推奨される導入療法は、CD38抗体薬のダラツムマブ(DARA)とメルファラン+プレドニゾロン+ボルテゾミ
ブ(MPB)との4剤併用(DARA+MPB)療法、あるいは、ダラツムマブとレナリドミド+デキサメタゾン(DARA+Ld)の3剤併用療法です。
何らかの理由でダラツムマブが使えない場合には、ボルテゾミブ+デキサメタゾン(Bd)かMPB療法、あるいはLd療法など新規薬剤を用いた2~3剤併用療法を行います。
ダラツムマブ、ボルテゾミブは注射薬(点滴薬)、レナリドミド、デキサメタゾン、プレドニゾロンは内服薬です。メルファランには内服薬と注射薬があり、MPB療法では、内服薬を用います。MPB療法は一般的には9コース、Ld療法は18コース行います。
完全寛解になるなど一定の治療効果が得られたら休薬して経過観察、あるいは、新規薬剤を用いた維持療法を行います。
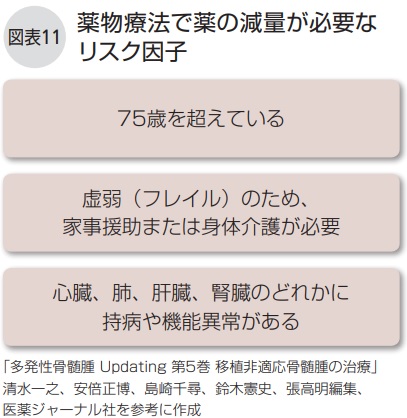
体力のない高齢者や心臓や腎臓に持病のある人などは薬の量を減らし、重い副作用を起こさないように気をつけながら病状をコントロールすることが重要です。
①図表11のリスク因子に1つでも当てはまる人、②図表11のリスク因子が1つ以上あり、重度の骨髄抑制(貧血、白血球・好中球・血小板の減少)が起こったことがある人には、ヨーロッパの専門家グループがこれまでの知見からつくった基準をもとに、薬の量を段階的に減らしていきます。また、骨髄腫による症状の出方や患者さんの持病、体力、希望に応じて、薬の組み合わせを変える場合もあります。
●入院が必要な治療とは
多発性骨髄腫の薬物療法は、内服薬も多く、外来での治療が増えています。
しかし、末梢血造血幹細胞の採取と移植のため、また多剤併用薬物療法1コース目は強い副作用が出ることがあるため、入院治療が一般的です。
最初に最も効果の高い治療法を
多発性骨髄腫に対しては、ここ数年、続々と新しい治療薬が登場しています。患者さんの中には、効果の高い治療法は、再発したときのために残しておいたほうがいいと考える人もいるのではないでしょうか。
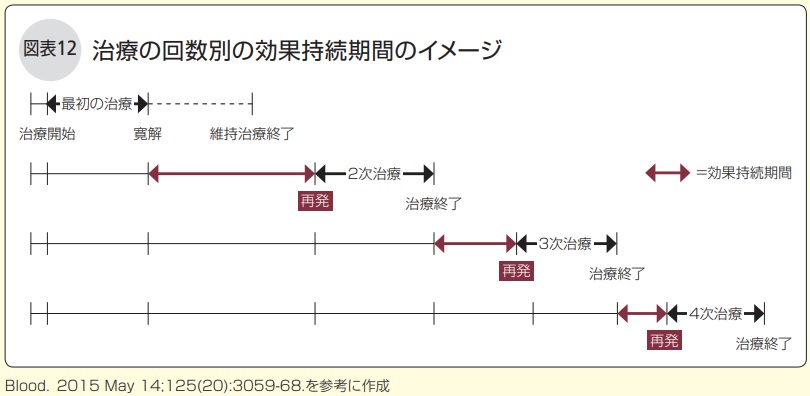
しかし、イギリス、フランス、ドイツなど欧州7か国で治療を受けた約5000人の患者さんの平均的な経過を分析した結果(図表12)では、効果が持続する期間は最初の治療が最も長く、治療を重ねるごとに、治療が奏効する患者さんの割合も減ることが示されています。一般的には、治療を重ねると、再発までの期間が短くなっていくのです。
したがって、効果の高い治療法は後回しにせず、その時点で最も信頼される標準治療を最初からしっかり行い、MRD陰性を目指すものです。
また、最初の治療で高い効果が得られれば、身体機能が維持され、これまでと同様の日常生活を長く続けることができます。QOL(生活の質)を高めることは、引き続き患者さんが効果的な治療法を選択し実施するうえでも、大切な要素になります。
参考資料
もっと知ってほしい多発性骨髄腫のこと 2021年版,pp.8-11



































